Myopathies des ceintures
Les myopathies des ceintures se manifestent de façons diverses allant d’une simple fatigabilité à des formes entraînant la perte de la marche, avec ou sans complications cardiaque et/ou respiratoire. Un suivi médical régulier permet de traiter à temps et limiter les conséquences de la maladie. Les thérapies innovantes sont des pistes de recherche en plein essor dans ces maladies.
Les myopathies des ceintures : qu’est-ce que c’est ?
Il s’agit de maladies génétiques rares qui touchent principalement les muscles (on parle de myopathie) dits « proximaux », c’est-à-dire ceux des épaules (ceinture scapulaire) et des hanches (ceinture pelvienne), qui diminuent progressivement de volume, s’affaiblissent et se régénèrent difficilement.
Elles apparaissent souvent avant l’âge de 20 ans, mais peuvent aussi débuter plus tardivement. Les premiers signes sont principalement des difficultés pour courir, pour monter les escaliers et se relever du sol. Les chutes sont fréquentes. Paradoxalement, les mollets peuvent être hypertrophiés et paraître très musclés.
Comment fait-on le diagnostic ?
Il se base sur l’identification des muscles atteints (ceux des ceintures), l’évolution de la maladie, l’histoire familiale (transmission génétique) et, pour un diagnostic de certitude, un test génétique révélant une ou des mutations pathologiques dans des gènes spécifiques. Le diagnostic peut être complété par d’autres examensprise de sang, imagerie des muscles, électromyogramme, biopsie musculaire… La prise de sang permet de recueillir des cellules (notamment des globules blancs) pour les analyses génétiques, et de mesurer la concentration sanguine de l’enzyme musculaire créatine kinase (CPK). Le fragment de muscle prélevé par biopsie musculaire permet de rechercher des altérations du tissu musculaire caractéristiques des LGMD (hétérogénéité de tailles des fibres musculaires, infiltrations graisseuses, fibrose…) et d’identifier, dans certains cas, la protéine déficitaire responsable de la maladie.
Que peut-on faire ?
La prise en charge médicale des LGMD est pour l’instant uniquement symptomatique ; elle vise essentiellement à prévenir les complications, notamment au niveau des muscles et des articulations. Les recherches avancent pour trouver un traitement dit de fond, qui cible la cause de la maladie.
La prise en charge d’une myopathie des ceintures se conçoit au mieux dans le cadre de consultations pluridisciplinaires spécialisées dans les maladies neuromusculaires.
- Une surveillance annuelle est recommandée pour faire un bilan musculaire, orthopédique, cardiaque et respiratoire.
- La prise en charge orthopédique (kinésithérapie, appareillage) doit être précoce, régulière et adaptée à chaque situation individuelle. Elle permet de lutter contre les conséquences de la maladie, en maintenant, notamment, la souplesse des articulations.
- Des aides techniques (canne, support de bras, pince à long manche...) peuvent aider à réaliser les gestes de la vie quotidienne que la gêne musculaire rend difficiles ou impossibles. Un scooter électrique ou un fauteuil roulant permettent de retrouver l’autonomie dans ses déplacements.
- Lorsqu’il existe une atteinte des muscles respiratoires, celle-ci nécessite une prise en charge spécifique.
- Un suivi cardiologique régulier permet de mettre en route rapidement un traitement adapté (médicaments, pacemaker, défibrillateur) au cas où une atteinte cardiaque serait détectée par les examens médicaux.
- Le conseil génétique permet d’informer et d’accompagner une personne, ou une famille, sur le risque de développer ou de transmettre la maladie.
La carte d’urgence LGMD, mise en place par la filière FILNEMUS, présente les recommandations importantes pour la sécurité et la prise en charge médicale d’urgence de la personne.
Voir le Repères LGMD pour en savoir plus
VOIR LES AVANCÉES 2025 DANS LES MYOPATHIES DES CEINTURES
LGMD R1 ou LGMD 2A ?
Depuis la publication en 2018 de travaux du European Neuromuscular Centre (ENMC), les communautés médicale et scientifique utilisent pour les LGMD une dénomination et une classification mises à jour. Le nom des différentes formes de LGMD prend dès lors le format suivant : LGMD « D » ou « R » pour le mode de transmission (dominant ou récessif), suivi d’un chiffre, indiquant l’ordre de découverte, et du nom de la protéine en cause. Ainsi la « LGMD 2A » devient la « LGMD R1 liée à la calpaïne 3 » (souvent raccourci en « LGMD R1 »). Toutefois, les anciennes appellations sont encore quelques fois utilisées dans la littérature médico-scientifique ou par la communauté LGMD.
On distingue souvent six groupes au sein des LGMD :
• Anoctaminopathies : LGMD R12
• Calpaïnopathies : LGMD R1 et D4
• Collagénopathies : LGMD R22 et D5
• Dysferlinopathies : LGMD R2
• Dystroglycanopathies : LGMD R9, R11, R13, R14, R15, R16, R19, R20 et R24
• Sarcoglycanopathies : LGMD R3, R4, R5 et R6
Des essais cliniques pour trouver des traitements efficaces
Plusieurs stratégies thérapeutiques sont à l’étude afin d’agir sur les différents mécanismes pathologiques propres à chaque forme de LGMD.

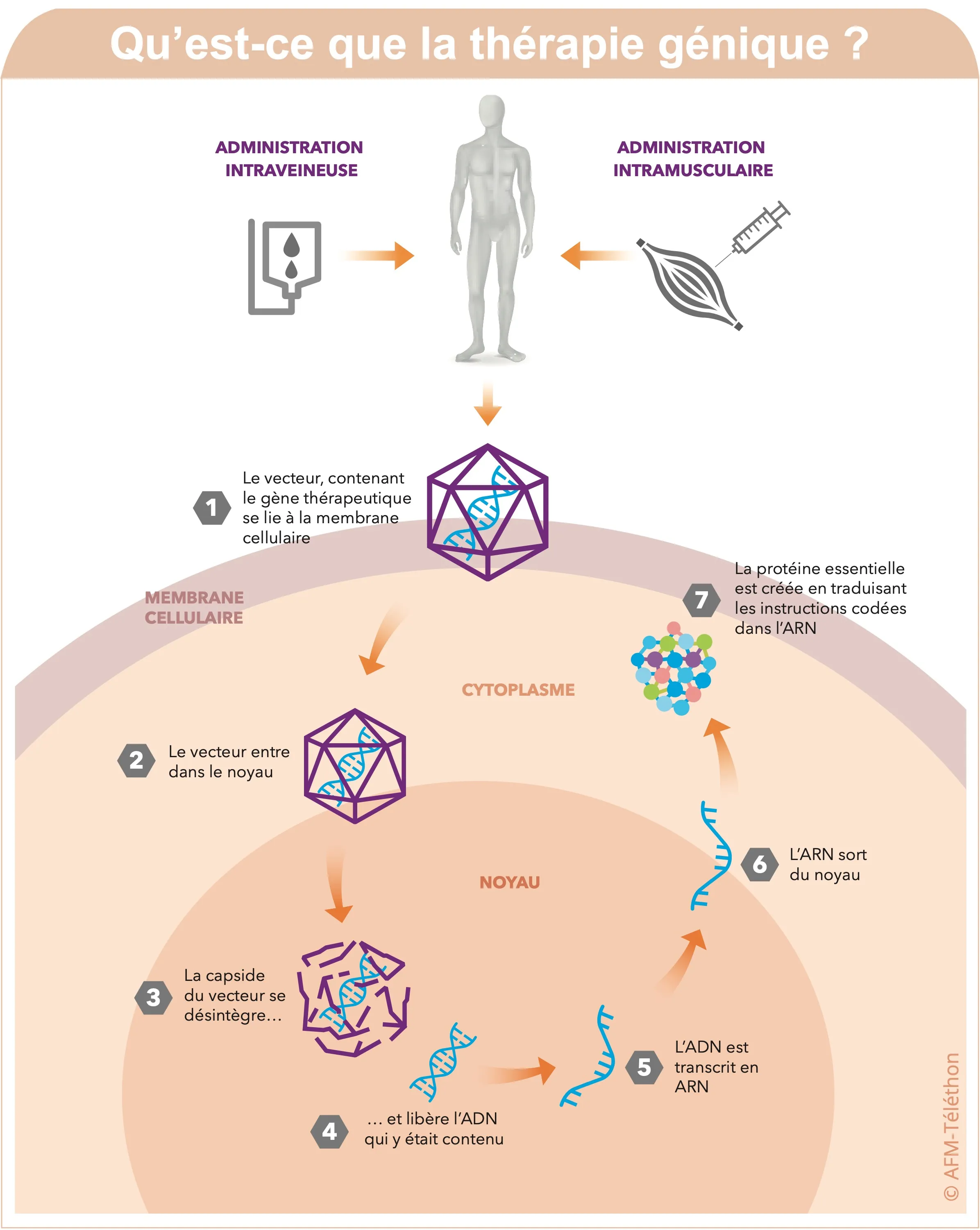
La thérapie génique
La thérapie génique consiste à insérer dans les cellules de la personne malade un « gène-médicament » afin d’apporter une copie fonctionnelle du gène déficient en cause dans la maladie. Il y a aujourd’hui plusieurs essais cliniques de thérapie génique dans les LGMD, avec des résultats intermédiaires encourageants.
• Dans la LGMD R2 liée à DYSF, après un premier essai clinique montrant la bonne tolérance du produit de thérapie génique SRP-6004, Sarepta Therapeutics a lancé en 2023 un second essai clinique appelé NAVIGENE. L’étude a pour objectif de confirmer la tolérance du produit, mais évalue aussi son efficacité, chez deux patients marchants.
• Dans la LGMD R3 liée à SGCA, une équipe avait publié en 2019 des résultats encourageants de la première administration chez l’homme d’un produit de thérapie génique, le SRP-9004. Les données montraient que cette approche était bien tolérée. En 2023, le produit a obtenu la désignation orpheline par l’Agence européenne des médicaments (EMA). Sarepta Therapeutics, a démarré en 2025 l’essai DISCOVERY, afin de récolter des données supplémentaires concernant l’innocuité et l’efficacité du SRP-9004.
• Dans la LGMD R4 liée à SGCB, les résultats préliminaires positifs concernant l’essai du produit de thérapie génique SRP-9003 avaient conduit Sarepta Therapeutics à lancer VOYAGENE, un essai clinique visant à générer des données complémentaires. Début 2024, la société de biotechnologie a annoncé poursuivre l’évaluation du produit chez l’Homme avec l’essai EMERGENE.
• Dans la LGMD R5 liée à SGCG, Atamyo Therapeutics, une société de biotechnologie créée en 2020 par Généthon sur la base des travaux de recherche de l’équipe d’Isabelle Richard, chercheuse au Généthon, a démarré début 2025 un essai multinational afin de tester la tolérance et l’innocuité du produit de thérapie génique ATA-200. Deux patients aux États-Unis ont déjà pu être traités avec ce candidat-médicament en avril et mai 2025.
Sarepta Therapeutics a lancé en 2025 aux États-Unis COMPASS, un essai clinique de thérapie génique pour évaluer les effets du candidat-médicament SRP-9005.
• Dans la LGMD R9 liée à FKRP, Atamyo Therapeutics a démarré en 2022 un essai clinique pour tester le produit de thérapie génique ATA-100. La biopharma a annoncé en 2025 avoir finalisé la première partie de la phase I/II de l’essai, et déterminé la quantité de produit donnant les meilleurs résultats. Cette dernière sera la dose utilisée pour la suite du développement clinique de l’ATA-100.
Aux États-Unis, Asklepios BioPharmaceutical (AskBio) évalue l’efficacité d’un autre gène-médicament, le LION-CS101. En mars 2025, après l’obtention de résultats préliminaires positifs, le laboratoire a annoncé avoir reçu les autorisations pour poursuivre l’évaluation du produit dans la deuxième cohorte de l’essai.
La thérapie pharmacologique
Elle utilise des petites molécules de nature différente (sucres, protéines, acides aminés…) pour corriger des processus biologiques (glycosylation, autophagie…) perturbés chez le malade. Dans la LGMD R9 liée à FKRP, deux molécules candidates sont à l’essai : le ribitol (BBP-418) et le sevasemten (EDG-5506). Sur la base des résultats positifs du ribitol, ML Bio Solutions a débuté en 2023 l’essai FORTIFY afin d’évaluer l’innocuité et l’efficacité du ribitol sur un plus grand nombre de malades. Le sevasemten, développé par Edgewise Therapeutics, est également en cours d’évaluation.
Depuis 2015, le laboratoire I-stem travaille sur des cellules modèles de myopathies des ceintures pour identifier des candidats-médicaments parmi des molécules déjà connues.
Les connaissances progressent
Depuis la découverte du gène de la calpaïne 3 en 1995 par l’équipe d’Isabelle Richard à Généthon, plus de 34 gènes différents ont été identifiés dans les LGMD. Les recherches ont montré que certains de ces gènes sont aussi impliqués dans d’autres formes de maladies neuromusculaires, notamment dans plusieurs formes de dystrophies musculaires congénitales, de myopathies distales ou de myopathies myofibrillaires.
Des études observationnelles sont en cours, et des bases de données sont mises en place pour mieux décrire les différentes formes de LGMD et leur évolution. Ces données sont particulièrement précieuses pour la préparation de futurs essais cliniques.
En France, cinq de ces études sont en cours sur les LGMD :
- L’étude EIDY évalue l’évolution de l’atteinte musculaire chez 80 personnes atteintes de LGMD, suivies pendant deux ans.
- L’étude GNT-015-FKRP, mise en route par le Généthon, cherche à mieux comprendre les mécanismes de la maladie et évalue l’évolution de la LGMD R9 liée à FKRP, chez 52 personnes suivies pendant deux ans, en prévision de futurs essais de thérapie génique.
- L’étude CALNATHIS évalue sur deux ans la perte de force des bras et des jambes chez 25 patients atteints de LGMD R1 liée à CAPN3.
- Le registre C3R, soutenu par l’AFM-Téléthon, est dédié aux calpaïnopathies, et recense des données médicales et génétiques issues du suivi, en consultation neuromusculaire de la filière Filnemus, d’enfants et d’adultes atteints de ces maladies en France.
- Le registre SARCO, développé également par l’AFM-Téléthon, rassemble des informations telles que l’âge de début de la maladie et ses manifestations, le gène en cause, le type de mutation, les résultats de certaines prises de sang, d’évaluations de la force musculaire des patients atteints de sarcoglycanopathies en France.
Le groupe d’intérêt AFM-Téléthon LGMD
Il rassemble des malades atteints de LGMD, experts de cette maladie. En plus du partage d’expériences, il apporte une information médicale et scientifique régulière sur son blog ou lors de journées d’information, en lien avec des médecins et chercheurs impliqués dans les LGMD.
https://lgmd.afm-telethon.fr/blog/





Comment évoluent-elles ?
Leur évolution est variable, mais en général relativement peu rapide. Les manifestations cliniques sont le plus souvent limitées aux muscles qui permettent le mouvement, aussi appelés muscles squelettiques. Selon le type de myopathie des ceintures (ou LGMD pour Limb-Girdle Muscular Dystrophy), il peut y avoir une atteinte des muscles de la respiration (difficultés respiratoires) et/ou du cœur (cardiomyopathie, troubles du rythme).
La perte de la force musculaire et les changements de structure (dystrophie) des muscles peuvent s’accompagner d’un enraidissement de ces derniers et des articulations (on parle de rétractions) qui peut entraîner des déformations articulaires (scoliose, colonne raide…).
Avec le temps, la marche peut devenir difficile, voire impossible dans certaines formes (notamment au sein des sarcoglycanopathies), tandis que d’autres sont assez peu ou pas évolutives, et les malades peuvent conserver la marche (comme dans les anoctaminopathies).
À quoi sont-elles dues ?
Trente-quatre formes de LGMD ont été répertoriées à ce jour. Elles sont dues à des anomalies pathologiques présentes dans autant de gènes indispensables au bon fonctionnement des muscles. Héréditaires, les LGMD se transmettent principalement de manière autosomique récessive (29 formes), et plus rarement sur le mode autosomique dominant (5 formes). Dans certains cas, les LGMD peuvent être dues à des mutations dites « de novo », qui n’étaient présentes chez aucun des parents.
Il est difficile de savoir combien de personnes sont touchées, mais on estime qu’environ 1 à 3 personnes sur 125 000 sont concernées par la maladie, toutes formes de LGMD confondues.