SMA : de nouveaux résultats d’essais cliniques

Tour d’horizon des derniers résultats d’essais annoncés ou publiés dans l’amyotrophie spinale proximale liée à SMN1.
L’évaluation des traitements déjà disponibles ou en cours de développement se poursuit dans l’amyotrophie spinale proximale liée à SMN1 (SMA).
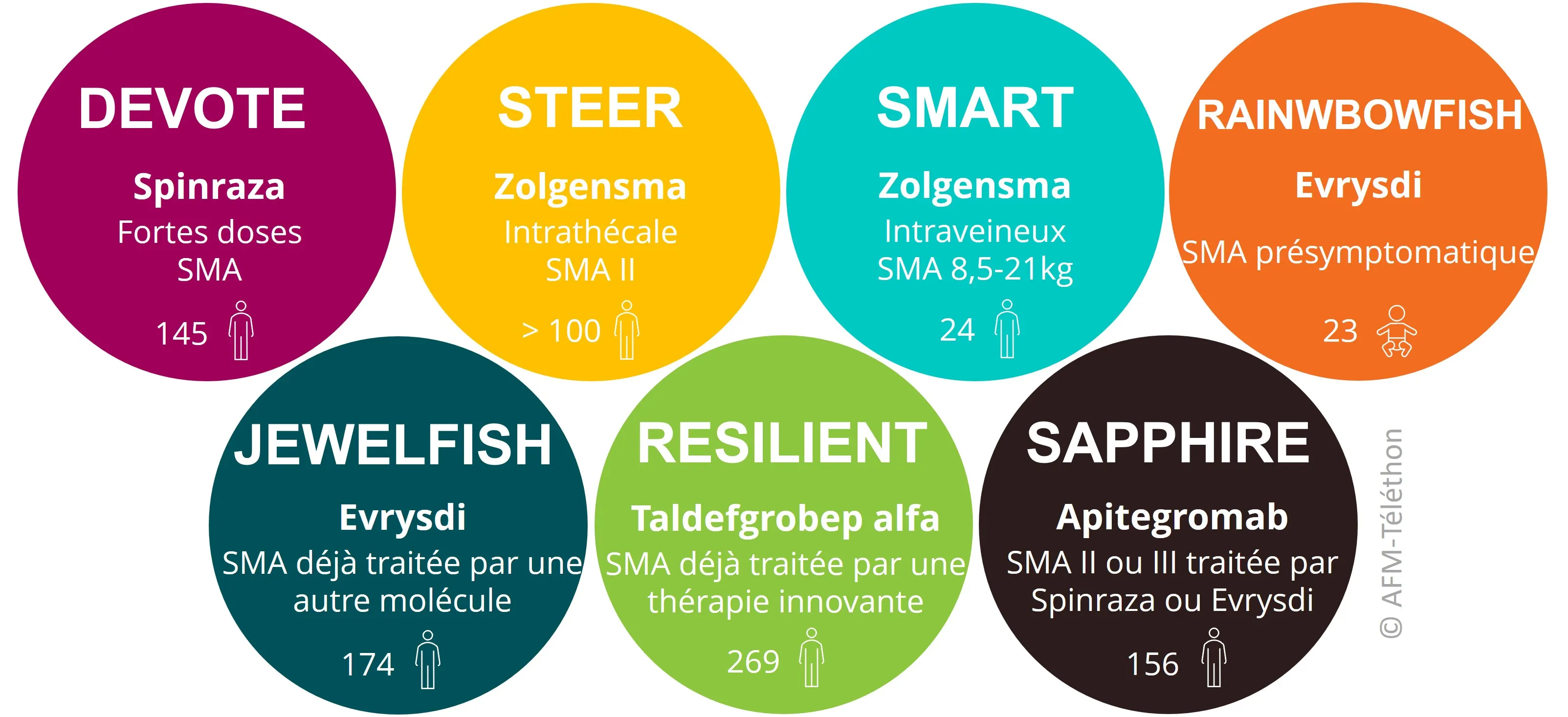
De plus fortes doses de Spinraza
De nouveaux résultats de l’essai DEVOTE ont mis en évidence les effets bénéfiques de plus fortes doses (50 ou 28 mg) du Spinraza (nusinersen) que celle utilisée actuellement (12 mg) chez des participants atteints de SMA ayant déjà été traités avant ou non. Alors que l’essai continue, le laboratoire Biogen, qui développe le médicament, envisage de déposer des demandes réglementaires dans le monde entier pour l’utilisation de doses plus élevées du nusinersen. Elles devraient permettre notamment d’utiliser des doses plus adaptées au poids des malades ou d’espacer les injections.
Voir le communiqué de presse de Biogen (en anglais).
Le Zolgensma, en intrathécale ou chez des enfants au poids plus élevé
L’administration du produit de thérapie génique par voie intrathécale, et non en intraveineux comme dans son indication actuelle, a été évaluée dans le cadre de l’essai STEER auprès de plus de 100 patients atteints de SMA de type II, âgés entre 2 et 18 ans, capables de s’asseoir mais pas de marcher seuls, et n’ayant reçu aucun traitement innovant. Dans cet essai de phase III, randomisé, en double aveugle, une partie des participants a reçu une procédure « factice » (sham procedure) qui imite l’injection à l’endroit où elle est normalement effectuée, mais qui est réalisée sans le produit (placebo). Après un an, tous les patients qui avaient reçu la procédure factice ont reçu le Zolgensma en administration intrathécale (avec une période de suivi de 3 mois), et inversement.
Des résultats à un an de cet essai communiqués par Novartis montrent des bénéfices cliniques chez les enfants traités, en comparaison à ceux ayant reçu la procédure factice, avec une amélioration de la fonction motrice et un ralentissement de la progression de la maladie. L’administration intrathécale du produit a par ailleurs été bien tolérée.
Voir le communiqué de presse de Novartis (en anglais).
Lors de l’essai SMART d’une durée d’un an, le Zolgensma a été administré par voie intraveineuse à 24 enfants symptomatiques, pesant de 8,5 à 21 kg et qui pour certains avaient déjà bénéficié d’une autre thérapie innovante (Spinraza ou Evrysdi). Les résultats de cet essai ont mis en évidence, après un an de traitement, la bonne tolérance et l’efficacité du produit dans cette population pédiatrique. Les fonctions motrices de la plupart des participants sont restées stables ou se sont améliorées.
Voir le résumé de l’article (en anglais).
L’Evrysdi, en présymptomatique ou chez des patients déjà traités
Des premiers résultats positifs de l’essai RAINBOWFISH qui concerne 23 nouveau-nés traités en présymptomatiques, avant l’âge de 6 semaines, ont été communiqués par le laboratoire Roche. Après deux ans de traitement, tous les enfants sont capables de s’asseoir seul, de s’alimenter par la bouche et d’avaler, sans recours à une ventilation permanente. La majorité a la capacité de marcher seul.
Voir le communiqué de presse de Roche (en anglais).
L’essai JEWELFISH a évalué pendant deux ans la sécurité d’utilisation, la tolérance et le devenir dans l'organisme (pharmacocinétique) de l’Evrysdi (risdiplam) chez 174 personnes atteintes de SMA, âgées de 6 mois à 60 ans, déjà traitées soit par Spinraza, Zolgensma, olésoxime ou RG7800. Après deux ans de traitement, les résultats publiés ont souligné la bonne tolérance du médicament ainsi que la présence de protéine SMN (protéine manquante dans la maladie) dans le sang. Une extension de cet essai est en cours pour suivre les effets du produit à plus long terme.
Voir le résumé de l’article (en anglais).
Les anti-myostatines, en complément des trois traitements autorisés
Des nouvelles du taldefgrobep alfa, dont l’essai RESILIENT évaluait son efficacité pendant un an chez 269 personnes atteintes de SMA déjà sous Spinraza, Zolgensma ou Evrysdi ont été partagées par Biohaven. Ce produit n’a pas réussi à démontrer son efficacité en comparaison d’un placebo sur la mesure de la fonction motrice (MFM-32), critère principal de l’essai. D’autres analyses des résultats sont en cours.
Voir le communiqué de presse de Bihaven (en anglais).
Dans le cadre de l’essai SAPPHIRE, les effets d’un double traitement associant l’apitegromab avec le Spinraza ou l’Evrysdi chez des patients atteints de SMA de type II ou III s’avèrent positifs, avec une amélioration de la fonction motrice après un an de traitement, en comparaison du groupe placebo.
Voir le communiqué de presse de Scholar Rock (en anglais).
Voir aussi la page des Essais cliniques dans la SMA en cours ou en préparation en France
